இண்டியம்Tt ya au waC ineCcimaqh hi 234n uzuT N506 Rrf
| |||||||||||||||||||
| பொது | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| பெயர், குறி எழுத்து, தனிம எண் |
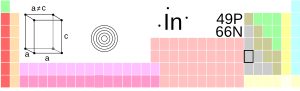
இண்டியம், In, 49 | ||||||||||||||||||
| வேதியியல் பொருள் வரிசை |
குறை மாழைகள் | ||||||||||||||||||
| நெடுங்குழு, கிடை வரிசை, வலயம் |
13, 5, p | ||||||||||||||||||
| தோற்றம் | siபளபளப்பான வெண் சாம்பல் 
| ||||||||||||||||||
| அணு நிறை (அணுத்திணிவு) |
114.818(3) g/mol | ||||||||||||||||||
| எதிர்மின்னி அமைப்பு |
[Kr] 4d10 5s2 5p1 | ||||||||||||||||||
| சுற்றுப் பாதையிலுள்ள எதிர்மின்னிகள் (எலக்ட்ரான்கள்) |
2, 8, 18, 18, 3 | ||||||||||||||||||
| இயல்பியல் பண்புகள் | |||||||||||||||||||
| இயல் நிலை | திண்மம் | ||||||||||||||||||
| அடர்த்தி (அறை வெ.நி அருகில்) |
7.31 கி/செ.மி³ | ||||||||||||||||||
| உருகுநிலையில் நீர்மத்தின் அடர்த்தி |
7.02 g/cm³ | ||||||||||||||||||
| உருகு வெப்பநிலை |
429.75 K (156.60 °C, 313.88 °F) | ||||||||||||||||||
| கொதி நிலை | 2345 K (2072 °C, 3762 °F) | ||||||||||||||||||
| நிலை மாறும் மறை வெப்பம் |
3.281 கி.ஜூ/மோல் (kJ/mol) | ||||||||||||||||||
| வளிமமாகும் வெப்ப ஆற்றல் |
231.8 கி.ஜூ/மோல் | ||||||||||||||||||
| வெப்பக் கொண்மை |
(25 °C) 26.74 ஜூ/(மோல்·K) J/(mol·K) | ||||||||||||||||||
| |||||||||||||||||||
| அணுப் பண்புகள் | |||||||||||||||||||
| படிக அமைப்பு | tetragonal | ||||||||||||||||||
| ஆக்சைடு நிலைகள் |
3 (இருதன்மை ஆக்ஸைடு) | ||||||||||||||||||
| எதிர்மின்னியீர்ப்பு | 1.78 (பௌலிங் அளவீடு) | ||||||||||||||||||
| மின்மமாக்கும் ஆற்றல் |
1st: 558.3 kJ/(mol | ||||||||||||||||||
| 2nd: 1820.7 kJ/mol | |||||||||||||||||||
| 3rd: 2704 kJ/mol | |||||||||||||||||||
| அணு ஆரம் | 155 பிமீ | ||||||||||||||||||
| அணுவின் ஆரம் (கணித்) |
156 pm | ||||||||||||||||||
| கூட்டிணைப்பு ஆரம் | 144 pm | ||||||||||||||||||
| வான் டெர் வால் ஆரம் |
193 பி.மீ (pm) | ||||||||||||||||||
| வேறு பல பண்புகள் | |||||||||||||||||||
| காந்த வகை | தரவு இல்லை | ||||||||||||||||||
| மின் தடைமை | (20 °C) 83.7 nΩ·m | ||||||||||||||||||
| வெப்பக் கடத்துமை |
(300 K) 81.8 வாட்/(மீ·கெ) W/(m·K) | ||||||||||||||||||
| வெப்ப நீட்சி | (25 °C) 32.1 மைக்.மீ/(மி.மீ·கெ) µm/(m·K) | ||||||||||||||||||
| ஒலியின் விரைவு (மெல்லிய கம்பி வடிவில்) |
(20 °C) 1215 மீ/நொடி | ||||||||||||||||||
| யங்கின் மட்டு | 11 GPa | ||||||||||||||||||
| மோவின்(Moh's) உறுதி எண் | 1.2 | ||||||||||||||||||
| பிரிநெல் உறுதிஎண் Brinell hardness]] |
8.83 MPa (மெகாபாஸ்) | ||||||||||||||||||
| CAS பதிவெண் | 7440-74-6 | ||||||||||||||||||
| குறிபிடத்தக்க ஓரிடத்தான்கள் | |||||||||||||||||||
| |||||||||||||||||||
| மேற்கோள்கள் | |||||||||||||||||||
இண்டியம் (Indium) என்பது In என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு தனிமமாகும். அணு எண் 49 கொண்ட இத்தனிமத்தை பின் இடைநிலைத் தனிமம் என்று வகைப் படுத்துகிறார்கள். புவி மேலோட்டில் மில்லியனுக்கு 0.21 பகுதிகள் இண்டியம் தனிமம் காணப்படுகிறது. மிகவும் மென்மையான இத்தனிமத்தை தேவைக்கேற்றார் போல உருவத்தை மாற்றிக் கொள்ள இயலும். சோடியம் மற்றும் காலியம் தனிமங்களைக் காட்டிலும் இண்டியத்தின் உருகுநிலை அதிகமாகும். ஆனால் இலித்தியம் மற்றும் வெள்ளீயம் தனிமங்களைக் காட்டிலும் குறைவான உருகுநிலை கொண்டதாகும். வேதியியல் ரீதியாக இண்டியமானது காலியம் மற்றும் தாலியத்தை ஒத்திருக்கிறது. பெரும்பாலும் இவ்விரண்டு தனிமங்களுக்கு இடையிலான பண்புகளை இண்டியம் வெளிப்படுத்துகிறது[1]. 1863 ஆம் ஆண்டு பெர்டினாண்டு ரெயிச் மற்றும் இயரோனிமசு தியோடர் ரிக்டர் நிறமாலையியல் செயல் முறைகள் மூலம் இண்டியத்தைக் கண்டறிந்தனர். நிறமாலையின் கருநீல வரிகளில் இத்தனிமம் தென்பட்டதால் இதற்கு இண்டியம் எனப்பெயரிடப்பட்டது. 1864 ஆம் ஆண்டில் இண்டியம் தனித்துப் பிரித்தெடுக்கப்பட்டது.
துத்தநாக சல்பைடு தாதுவில் இண்டியம் சிறிதளவு காணப்படுகிறது. துத்தநாகத்தை தூய்மைப்படுத்தும் செயல் முறையில் ஒரு உடன் விளைபொருளாக இண்டியம் கிடைக்கிறது. குறைக்கடத்தி தொழிற்சாலைகளில் இத்தனிமத்தை பயன்படுத்துகிறார்கள். குறிப்பாக பற்றாசு போன்ற தாழ் உருகுநிலை கொண்ட கலப்பு உலோகங்களில் இண்டியம் பயன்படுத்தப்படுகிறது. மேலும் உயர் வெற்றிட முத்திரைகள், கண்ணாடிகள் மீது பூசப்பயன்படுத்தும் இண்டியம்வெள்ளீய ஆக்சைடு உற்பத்திக்கு இண்டியம் பயன்படுகிறது. இரத்த ஓட்டத்தில் இண்டியம் சேர்மங்களைச் செலுத்தினாலும் அவை சிறிதலவு மட்டுமே நச்சுத்தன்மையைக் காட்டுகிறது மற்றும் எந்தவிதமான உயிர்னச் செயல்பாடுகளிலும் இது பங்கேற்பதில்லை. சுவாசம், ஈர்ப்பு முறைகளால் இண்டியம் உடலுக்குள் செல்வதில்லை. உட்செலுத்துதல் மூலம் மட்டுமே இவை உடலுக்குள் செல்கின்றன.
பொருளடக்கம்
- 1 பண்புகள்
- 1.1 இயற்பியல் பண்புகள்
- 1.2 வேதியியல் பண்புகள்
- 2 வரலாறு
- 3 கிடைக்கும் அளவும் பயன்கொள்ளும் அளவும்
- 4 மேற்கோள்கள்
- 5 வெளி இணைப்புகள்
பண்புகள்[தொகு]
இயற்பியல் பண்புகள்[தொகு]
இண்டியம் தனிமம் வெள்ளி போன்ற வெண்மையான நிறங்கொண்டதாகும். மிகவும் பளபளப்பான இத்தனிமம் பின் இடைநிலைத் தனிமங்கள் வகையில் ஒரு உறுப்பினராகும் [2]. மிகவும் மென்மையான இத்தனிமத்தை கத்தியைக் கொண்டு வெட்டலாம். மோவின் கடினத்தன்மை மதிப்பு 1.2 ஆகும். தனிமவரிசை அட்டவனையின் 13 ஆவது குழுத் தனிமங்களின் குடும்பத்தில் இண்டியமும் ஓரு உறுப்பினர் ஆகும். காலியம் போல் இதுவும் கண்ணாடியில் சற்று பற்றி "நனை"க்கவல்ல பொருள் (பார்க்க: நனைப்புமை).இண்டியத்தின் பண்புகள் நெடுக்க வரிசையில் அடுத்துள்ள தனிமங்களான காலியம் மற்றும் தாலியம் இவற்றின் பண்புகளுக்கு இடைப்பட்டதாக உள்ளது. வெள்ளீயம் போலவே இன்டியத்தை வளைக்கும் போதும் படிகப்பகிர்தல் காரணமாக ஓர் உயர்ந்த சத்தம் கேட்கிறது. இலேசான காலியத்தைக் காட்டிலும் உயர்ந்த 156.60 ° செல்சியசு என்ற உருகுநிலையும் கனமான தாலியத்தைக் காட்டிலும் உயர்ந்த உருகுநிலையும் கொண்டதாக உள்ளது[3]. கொதிநிலையைப் பொறுத்தவரை 2072 பாகை செல்சியசு என்ற கொதிநிலையை இண்டியம் பெற்றுள்ளது. இது தாலியத்தைக் காட்டிலும் அதிகமாகவும் காலியத்தைக் காட்டிலும் குறைவானது ஆகும். இப்பண்பு தனிம வரிசை அட்டவணையின் கொதிநிலைப் பண்புகளின் பொதுப் போக்கிற்கு மறுதலையாக உள்ளது. ஆனால் இதர பின் இடைநிலைத் தனிமங்களின் போக்கிற்கு இசைவாக உள்ளது. சில எலக்ட்ரான்களின் உள்ளடங்காப் பண்புடன் கொண்டுள்ள உலோகப் பிணைப்பின் வலிமை இன்மை இதற்குக் காரணமாகும்[4].
7.31 கிராம்/செ.மீ3 என்ற இண்டியத்தின் அடர்த்தியும் காலியத்தைக் காட்டிலும் அதிகம் மற்றும் தாலியத்தைக் காட்டிலும் குறைவாகும். 3.41 கெல்வின் என்ற வெப்பநிலைக்கு கீழ் இண்டியம் ஒரு மீகடத்தியாக மாறுகிறது. திட்டவெப்பம் மற்றும் அழுத்தத்தில் இண்டியம் முகமைய நாற்கோணக வடிவில் இடக்குழு I4/எம் எம் எம் அளவில் படிகமாகிறது. (a = 325 பைக்கோமீட்டர், c = 495 பைக்கோமீட்டர்) ஓர் உருக்குலைந்த முகமைய கட்டமைப்பாகத் தோன்றுகிறது. ஒவ்வொரு இண்டியம் அணுவும் 324 மைக்கோமீட்டர் இடைவெளியில் நான்கு அண்டை உறுப்பினர்களையும், 336 மைக்கோமீட்டர் இடைவெளியில் எட்டு சற்று தொலைவிலும் பெற்றுள்ளது [5].
அரிதில் கானப்படும் ஒரு பண்பு, இதன் பரவலாக கிடைக்கும் ஓரிடத்தான் சிறிதளவு கதிரியக்கம் கொண்ட ஒன்று. ஆனால் அது மிகவும் மெதுவாக சிதைந்து வெள்ளீயம் ஆக மாறுகின்றது. இதன் அரைவாழ்வு 4.41×1014 ஆண்டுகள். இது அண்டம் தோன்றிய காலத்தைவிட 10,000 மடங்கு அதிகமானது. இயற்கையில் கிடைக்கும் தோரியம் என்னும் கதிரியக்கத் தனிமத்தை விட 50,000 மடங்கு அதிகமான கால அளவு. இந்த கதிரியக்கம் சிறியதென்பதால் கெடுதல் தராத ஒன்று ஆகும். இண்டியமானது, காமியம் போல கூடக்கூட நச்சுத்தன்மை பெறாத ஒரு நெடுங்குழு 5 ஐச் சேர்ந்த ஒரு தனிமம் ஆகும்.
வேதியியல் பண்புகள்[தொகு]
இண்டியம் 49 எலக்ட்ரான்களைக் கொண்டு [Kr]4d105s25p1 என்ற எலக்ட்ரான் ஒழுங்கமைப்புடன் காணப்படுகிறது. சேர்மங்களாக மாறும் போது இண்டியம் மூன்று வெளிக்கூட்டு எலக்ட்ரான்களை வழங்கி இண்டியம்(III), In3+ ஆக மாறுகிறது. சில நிகழ்வுகளில் 5s எலக்ட்ரான்கள் வழங்கப்படுவதில்லை. இதனால் இண்டியம் (I) In+ உருவாகிறது. ஒற்றை இணைதிற நிலையின் நிலைப்புத்தன்மை மந்த இணை விளைவுகளுக்கு காரணம் ஆகும். கன உலோகங்களில் 5s சுற்றுப்பாதையின் சார்பியல் விளைவுகள் நிலைநிறுத்துகின்றன. இண்டியத்தின் ஒத்தவரிசையில் அமைந்துள்ள கன உலோகமான தாலியம் வலிமையான சார்பியல் விளைவைக் காட்டுகிறது இதனால் தாலியம்(III) நிலையைக் காட்டிலும் தாலியம்(I) நிலைக்கு அதிக நிகழ்வாய்ப்பு உள்ளது[6]. இதேபோல இண்டியத்தின் ஒத்தவரிசையில் அமைந்துள்ள இலேசான உலோகமான காலியம் பொதுவாக +3 என்ற ஆக்சிசனேற்ற நிலையைக் காட்டுகிறது. தாலியம் வலிமையான ஆக்சிசனேற்றியாகவும் இண்டியம் அவ்வாறில்லாததற்கும் இதுவே காரணமாகும். பல இண்டியம்(I) சேர்மங்கள் வலுவான ஒடுக்கும் முகவர்களாக உள்ளன. இண்டியம்(I) ஆக்சைடு மற்றும் ஐதராக்சைடுகள் அதிக காரமாகவும் இண்டியம்(III) ஆக்சைடு மற்றும் ஐதராக்சைடும் அதிக அமிலத்தன்மையும் கொண்டுள்ளன.
வரலாறு[தொகு]
கிடைக்கும் அளவும் பயன்கொள்ளும் அளவும்[தொகு]

நில உருண்டையில் ஏறத்தாழ 0.1 மிஒப (ppm) (மிஒப (ppm) = மில்லியலின் ஒரு பங்கு) உள்ளதாக கணக்கிடப்பட்டுள்ளது. எனவே இது ஏறத்தாழ வெள்ளி போலும் அருகியே கிடைக்கும் ஒரு பொருள். ஆனாலும் ஒரு குறிப்பிட்ட எடைக்கு வெள்ளியை விட இண்டியம் மூன்று மடங்கு விலை உயர்ந்தது. 1924 ஆம் ஆண்டு வரை உலகம் முழுவதிலும் மொத்தம் ஏறத்தாழ ஒரேஎ ஒரு கிராம் அளவே இண்டியம் பிரித்து எடுக்கப்பட்டிருந்தது. அண்மையில் கனடாவில் பிரிட்டிஷ் கொலம்பியாவில் உள்ள டெக் கோமின்க்கோ தூய்ப்பிரிப்பு ஆலையில் 2005 ஆம் ஆண்டு 32,500 கிலோ கிராம் பிரித்தெடுத்திருக்கிறார்கள் (2004 ஆம் ஆண்டில் 42,800 கி.கி, 2003 ஆம் ஆண்டில் 36,100 கி.கி). இண்டியம் துத்தநாகம் பிரித்தெடுக்கும் தொழிலில் துணைவிளை பொருளாக கிடைக்கின்றது. 2002 ஆம் ஆண்டு ஒரு கி.கி $94 இருந்தது, ஆனால் 2005 ஆம் ஆண்டு இண்டியத்தின் விலை ஒரு கி.கி ஐக்கிய அமெரிக்க டாலர் $900/kg ஆக உயர்ந்துள்ளது.
மேற்கோள்கள்[தொகு]
- ↑ W. M. Haynes (2010). David R. Lide. ed. CRC Handbook of Chemistry and Physics: A Ready-reference Book of Chemical and Physical Data. CRC Press. பன்னாட்டுத் தரப்புத்தக எண்:978-1-4398-2077-3. https://books.google.com/books?id=oROqPwAACAAJ.
- ↑ Alfantazi, A. M.; Moskalyk, R. R. (2003). "Processing of indium: a review". Minerals Engineering 16 (8): 687–694. doi:10.1016/S0892-6875(03)00168-7.
- ↑ Dean, John A. (523). Lange's handbook of chemistry (Fifteenth edition). McGraw-Hill, Inc.. பன்னாட்டுத் தரப்புத்தக எண்:0-07-016190-9.
- ↑ Greenwood and Earnshaw, p. 222
- ↑ Greenwood and Earnshaw, p. 252
- ↑ Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (1985). "Thallium" (in de). Lehrbuch der Anorganischen Chemie (91–100 ). Walter de Gruyter. பக். 892–893. பன்னாட்டுத் தரப்புத்தக எண்:3-11-007511-3.
வெளி இணைப்புகள்[தொகு]
| விக்கிமீடியா பொதுவகத்தில் Indium என்னும் தலைப்புடன் தொடர்புடைய பல ஊடகக் கோப்புகள் உள்ளன. |
- தனிமங்கள் வலையில் இண்டியம் பற்றி (ஆங்கில மொழியில்)
- இண்டியம் தொழில்நிறுவனம் வலைத்தளம் (ஆங்கில மொழியில்)
- Reducing Agents > Indium low valent
| தனிம அட்டவணை | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||